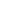
華夏源類器官:2024年1月-5月獲批消化系統抗腫瘤藥物匯總
根據統計數據,在全球范圍內,前五種造成患者死亡數量最多的腫瘤中,有3類屬于消化系統腫瘤。消化系統的腫瘤包括食管癌、胃癌、結直腸癌、肝細胞瘤、膽道系統腫瘤和胰腺癌等。與其他類型的腫瘤患者相比,消化系統惡性腫瘤的患者生存情況更加令人擔憂。
近年來,消化系統腫瘤的治療突破不斷,尤其是以外科手術為核心的綜合療法的發展。同時,在抗腫瘤藥物研發方面,一些新藥的出現給消化系統腫瘤藥物研發領域和患者帶來了新的希望。本文對2024年1月-5月上市的消化系統腫瘤新藥做依次梳理,以饗讀者。
胃癌
01
替雷利珠單抗
商品名:百澤安
通用名:替雷利珠單抗、Tislelizumab
適應癥:G/GEJ
臨床試驗:RATIONALE-305
原研公司:百濟神州
獲批日期:2024.04.30
獲批機構:NMPA
2024年4月30日,NMPA批準替雷利珠單抗聯合氟尿嘧啶類和鉑類藥物化療用于局部晚期不可切除的或轉移性的G/GEJ腺癌的一線治療。
至此,替雷利珠單抗已有13項適應癥在國內獲批,涵蓋癌種包括經典型霍奇金淋巴瘤、尿路上皮癌、NSCLC、肝細胞癌(HCC)、實體瘤、食管鱗狀細胞癌(ESCC)、鼻咽癌、G/GEJ。
臨床數據:
本次獲批是基于一項隨機、雙盲、安慰劑對照的III期臨床研究RATIONALE-305(NCT03777657),該研究共納入997例晚期不可切除或轉移性G/GEJ腺癌患者,按照1:1比例隨機接受替雷利珠單抗聯合化療(n=501)或安慰劑聯合化療(n=496)治療。主要研究終點為OS。對PD-L1高人群進行預先指定的分層,隨后是ITT人群。
結果顯示,PD-L1 TAP平分≥5%的患者使用替雷利珠單抗聯合化療與安慰劑聯合化療相比,總生存期顯著改善,中位OS分別為17.2個月和12.6個月,中位PFS分別為7.2個月和5.9個月。
在ITT人群中,替雷利珠單抗組合安慰劑組的OS分別為15.0個月和12.9個月,中位PFS分別為6.9個月和6.2個月。
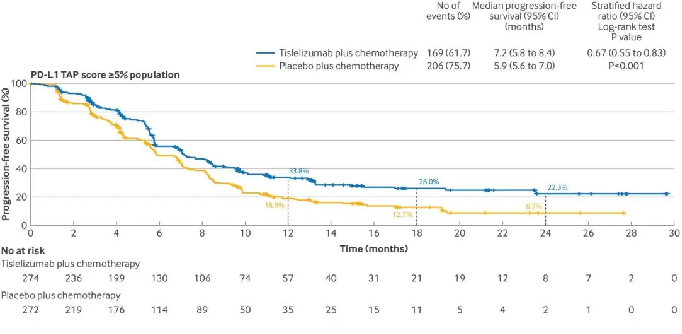
△ 替雷利珠單抗聯合化療對比安慰劑聯合化療在PD-L1 TAP≥5%人群的生存曲線和PFS數據。
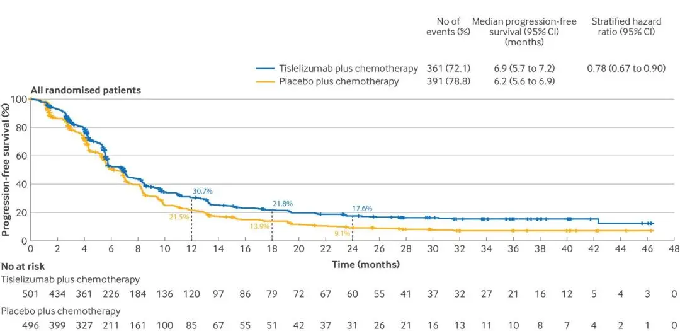
△ 替雷利珠單抗聯合化療對比安慰劑聯合化療在ITT人群的生存曲線和PFS數據。
2023年2月,替雷利珠單抗就已獲批用于聯合氟尿嘧啶類和鉑類藥物化療用于PD-L1高表達的局部晚期不可切除的或轉移性的G/GEJ腺癌的一線治療。本次獲批進而驗證了無論PD-L1表達如何,替雷利珠單抗聯合化療作為晚期胃癌的一線治療均可使患者獲益。
02
Zolbetuximab
商品名:Vyloy
通用名:Zolbetuximab、佐貝妥昔單抗
適應癥:CLDN18.2陽性胃癌
臨床試驗:SPOTLIGHT、GLOW
原研公司:安斯泰來
獲批日期:2024.03.26
獲批機構:MHLW
2024年3月26日,MHLW批準Zolbetuximab用于治療CLDN18.2陽性、不可切除、晚期或復發性胃癌患者。Zolbetuximab成為目前世界首個且唯一被批準的CLDN18.2靶向療法。
Claudin(CLDN)是正常組織緊密連接中重要的一種蛋白質,具有4個跨膜結構域,它參與細胞旁通透性和電導等過程的調節。
CLDN18.2在包含胃癌在內的消化道癌癥中高度表達。因此,CLDN18.2為治療胃癌、胰腺癌等實體腫瘤的有效靶標。
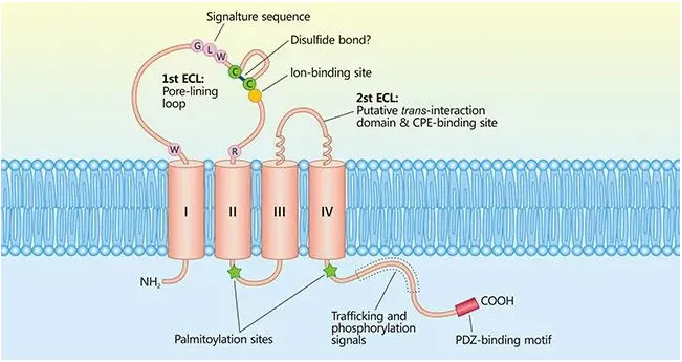
△ Claudin蛋白結構。
Zolbetuximab是一種IgG1單克隆抗體,在腫瘤細胞表面與CLDN18.2特異結合從而發揮抗腫瘤作用。
臨床前研究表明,這種結合作用通過激活兩種不同的免疫系統途徑——抗體依賴性細胞毒性(ADCC)和補體依賴性細胞毒性(CDC)誘導癌細胞死亡,以期達到腫瘤治療的目的。
臨床數據:
此次批準基于針對局部晚期不可切除或轉移性 HER2 陰性胃或胃食管連接部 (GEJ) 腺癌且腫瘤為 CLDN18.2 陽性的患者進行一線治療的3 期SPOTLIGHT(NCT03504397)和GLOW(NCT03653507)臨床試驗的結果。
SPOTLIGHT是一項全球、多中心、雙盲、隨機III期研究,GLOW(封閉招募)是一項全球、雙盲、3 期研究,與 SPOTLIGHT 同時進行,以確認在一線治療環境中在化療中添加佐爾貝妥昔單抗的療效。
SPOTLIGHT試驗結果顯示,接受Zolbetuximab與mFOLFOX6(一種包含奧沙利鉑、亞葉酸鈣和氟尿嘧啶的聯合化療方案)組合治療患者的PFS與OS在統計上有明顯改善。
Zolbetuximab組和安慰劑組的PFS分別為10.61個月和8.67個月,OS分別為18.23個月和15.54個月。與安慰劑組相比,Zolbetuximab組患者的疾病進展與死亡風險顯著降低24.9%,達成試驗主要終點。
GLOW試驗結果顯示,接受Zolbetuximab與CAPOX(一種包括卡培他濱和奧沙利鉑的聯合化療方案)組合療法患者的PFS在統計上顯著改善。Zolbetuximab組和安慰劑組的PFS分別為8.21個月和6.8個月。與安慰劑組相比,組合療法可降低患者疾病進展或死亡風險達31.3%。此外,組合療法還顯著延長患者的OS(試驗的關鍵次要終點),兩組OS分別為14.39個月和12.16個月,降低患者的死亡風險達22.9%。
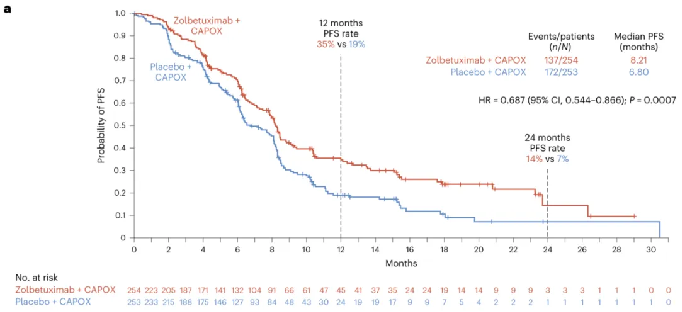
△ GLOW試驗中患者的PF。S結果。

△ GLOW試驗中患者的OS結果。
Zolbetuximab與mFOLFOX6或CAPOX聯用最常見的(≥20%)治療伴發不良反應(TEAE)是惡心、嘔吐、食欲下降、中性粒細胞減少和體重減輕。在臨床試驗中,不良反應可通過止吐藥、劑量中斷和輸注速度調整來控制。
03
舒格利單抗
商品名:擇捷美
通用名:舒格利單抗、Sugemalimab
適應癥:PD-L1表達(CPS≥5)G/GEJ
臨床試驗:GEMSTONE-303
原研公司:基石藥業
獲批日期:2024.03.15
獲批機構:NMPA
2024年3月15日,NMPA批準舒格利單抗聯合氟尿嘧啶類和鉑類藥物化療用于一線治療PD-L1表達(綜合陽性評分CPS≥5)的不可手術切除的局部晚期或轉移性G/GEJ患者。這是NMPA批準舒格利單抗的第五項適應癥。
臨床數據:
本次獲批是基于一項多中心、隨機、雙盲、安慰劑對照的III期臨床研究GEMSTONE-303,該研究旨在評估舒格利單抗聯合奧沙利鉑和卡培他濱作為一線治療無法手術切除的PD-L1表達(CPS≥5)的局部晚期或轉移性G/GEJ的療效和安全性。試驗的主要研究終點為研究者評估的PFS和OS。該研究是目前首個使用PD-L1單抗達成PFS和OS雙終點陽性的臨床研究。
結果顯示,舒格利單抗組對比安慰劑組在雙主要終點均有顯著改善,達到PFS和OS雙終點陽性且安全性良好可耐受。
PFS數據顯示,舒格利單抗組對比安慰劑組的中位PFS顯著改善,由研究者評估的中位PFS分別為7.6個月和6.1個月,降低34%疾病進展或死亡風險。PFS亞組分析顯示各亞組一致獲益,其中在PD-L1 CPS≥10的人群中,PFS獲益更顯著,PFS分別為7.79個月和5.52個。
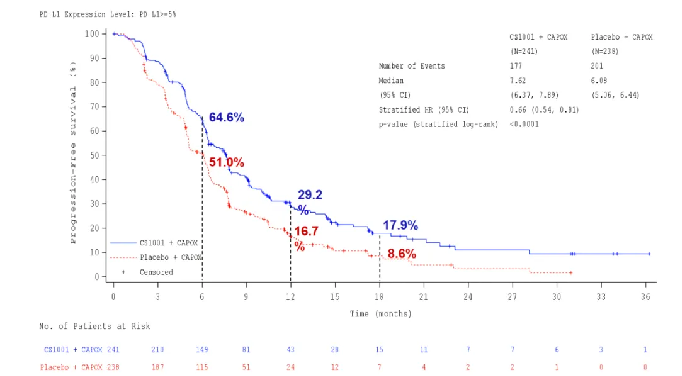
△ PD-L1 CPS≥5人群的PFS獲益結果。
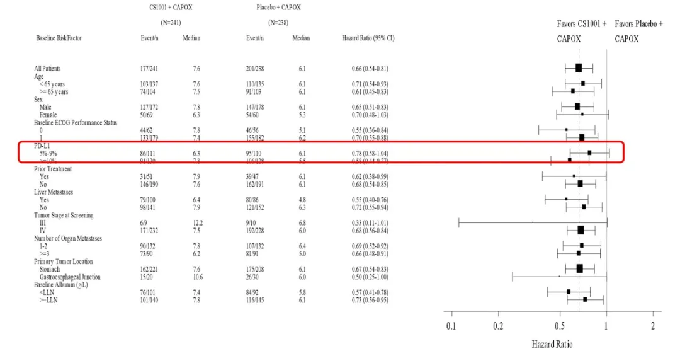
△ PFS亞組分析結果。
OS數據顯示,舒格利單抗組對比安慰劑組的中位OS延長近3個月,分別為15.6個月和12.6個月,降低死亡風險25%,其中,PD-L1 CPS≥10人群的OS獲益更顯著,中位OS延長5個多月,分別為17.81個月和12.45個月,降低死亡風險36%。此外,兩組12個月OS率分別為61.25%和52.02%,24個月OS率分別為29.9%和23.28%。
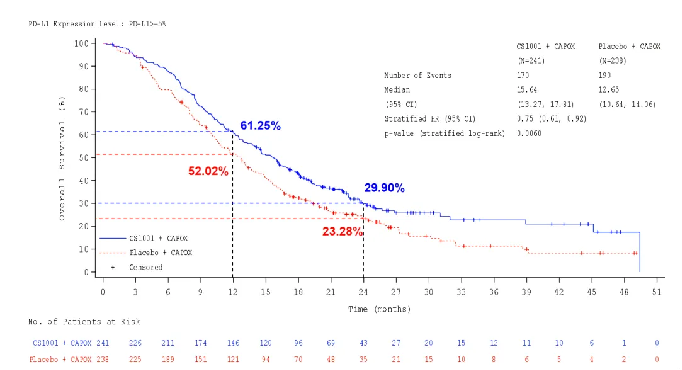
△ PD-L1 CPS≥5人群的OS獲益結果。
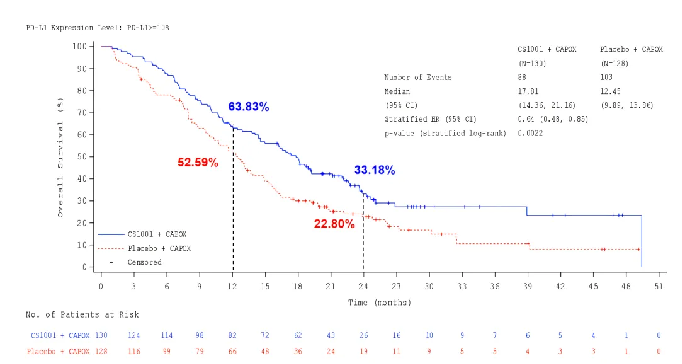
△ PD-L1 CPS≥10人群的OS獲益結果。
次要終點方面,舒格利單抗組與安慰劑組的ORR分別為68.6%和52.7%,其中,PD-L1 CPS≥10人群的ORR高達71.4%。中位DoR分別為6.87個月和4.63個月,舒格利單抗組可為晚期胃癌患者帶來更深程度的腫瘤緩解。
安全性方面,舒格利單抗組對比安慰劑組的3-5級相關AE的發生率分別為31.1%和28.7%,未觀察到新的安全信號,整體安全可耐受。
食管鱗狀細胞癌(ESCC)

01
替雷利珠單抗
商品名:百澤安
通用名:替雷利珠單抗、Tislelizumab
適應癥:ESCC
臨床試驗:RATIONALE 302
原研公司:百濟神州
獲批日期:2024.03.15
獲批機構:FDA
2024年3月15日,替雷利珠單抗獲FDA批準,作為單藥治療既往接受過系統化療(不含PD-1/L1抑制劑)后不可切除或轉移性ESCC成人患者。此次獲批標志著替雷利珠單抗在美國獲批首個適應癥。
臨床數據:
本次獲批是基于一項全球、隨機、開放性的III期臨床研究RATIONALE 302(NCT03430843),該研究旨在比較替雷利珠單抗單藥和研究者選擇的化療在不可切除、局部晚期或轉移性ESCC患者二線治療時的有效性和安全性。
結果顯示,替雷利珠單抗與化療相比顯著改善了患者的OS,中位OS分別為8.6個月和6.3個月。替雷利珠單抗組的6個月OS率為62.3%,化療組為51.8%;12個月OS率分別為37.4%和23.7%。在PD-L1表達≥10%人群中,替雷利珠單抗的總生存期更是達到了10.3個月。
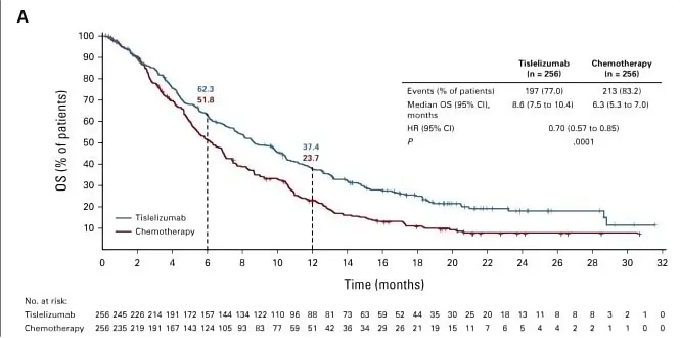
△ ITT人群的OS獲益結果。
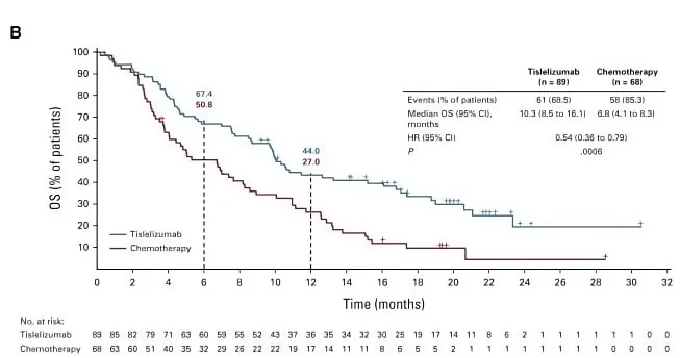
△ PD-L1 TAP≥10%人群的OS獲益結果。
肝細胞癌(HCC)

01
替雷利珠單抗
商品名:百澤安
通用名:替雷利珠單抗、Tislelizumab
適應癥:HCC
臨床試驗:RATIONALE 301
原研公司:百濟神州
獲批日期:2024.01.02
獲批機構:NMPA
2024年1月2日,替雷利珠單抗已正式獲批用于一線治療不可切除或轉移性HCC患者。截至目前,替雷利珠單抗已有13項適應癥獲得NMPA批準,是目前在中國獲批適應癥數量最多的PD-1抑制劑,涵蓋NSCLC、經典型霍奇金淋巴瘤、尿路上皮癌、HCC、食管鱗狀細胞癌、鼻咽癌、胃或胃食管結合部(G/GEJ)腺癌等癌種。
臨床數據:
此次獲批是基于RATIONALE 301研究( NCT03412773)的臨床試驗數據。該研究也是國際上首個獲得預期的陽性結果的替雷利珠單抗一線治療晚期不可切除肝細胞癌患者的前瞻性、隨機對照、關鍵性III期臨床試驗,旨在評估替雷利珠單抗相比與晚期HCC標準一線治療藥物索拉非尼的有效性和安全性,主要終點為兩個治療組OS的非劣效比較。
結果顯示,替雷利珠單抗與索拉非尼相比達到了預設的主要研究終點,即OS為非劣效性。替雷利珠單抗組的中位OS為15.9個月,而索拉非尼組的中位OS為14.1個月,死亡風險降低了15%,mOS延長了1.8個月,具有生存獲益的趨勢。
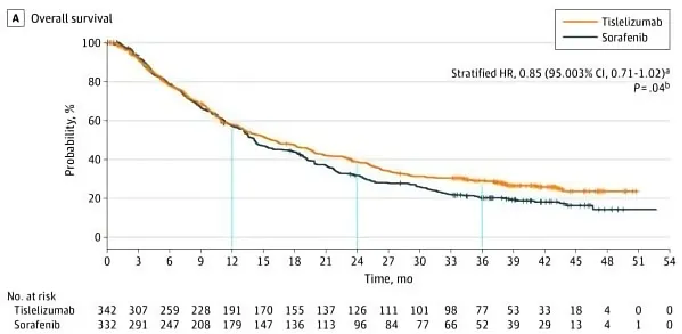
△ RATIONALE 301研究OS結果。
在腫瘤緩解方面,替雷利珠單抗組的ORR為14.3%,其中有將近3%的患者(10例)獲得了腫瘤完全緩解(CR),而索拉非尼組的ORR僅為5.4%。更為可喜的是,在DOR方面,替雷利珠單抗顯示出明顯的優勢,中位DOR達到了36.1個月。
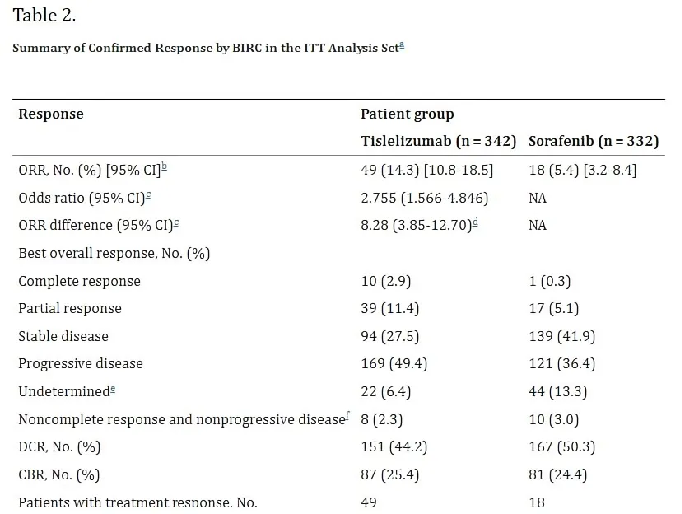
△ RATIONALE 301研究臨床數據。
膽道癌(BTC)

01
帕博利珠單抗
商品名:可瑞達、Keytruda
通用名:帕博利珠單抗、Pembrolizumab
適應癥:BTC
臨床試驗:KEYNOTE-966
原研公司:默沙東
獲批日期:2024.02.04
獲批機構:NMPA
2024年2月4日,帕博利珠單抗獲批用于聯合吉西他濱和順鉑用于局部晚期或轉移性BTC患者的一線治療。這是在中國獲批上市以來,帕博利珠單抗在國內獲批的第13項適應證。
臨床數據:
該適應證的獲批基于KEYNOTE-966研究(NCT04003636)結果。KEYNOTE-966為一項國際多中心、隨機、安慰劑對照的III期臨床研究,旨在評估帕博利珠單抗聯合吉西他濱/順鉑對比安慰劑聯合吉西他濱/順鉑治療既往未接受過系統治療的晚期BTC成人患者的療效和安全性,是首個程序性死亡受體1抑制劑的安慰劑對照研究,也是有關程序性死亡受體1或其配體檢查點抑制劑顯著改善晚期膽道惡性腫瘤患者總生存期且安全性可控的第2個研究。
結果顯示,中位隨訪29.5個月時,帕博利珠單抗組和安慰劑組的中位OS分別為12.7個月和10.9個月,存在顯著差異。兩組的12個月OS率分別為52%和44%,24個月OS率分別為25%和19%。兩組的中位PFS分別為6.5個月和5.6個月,中位DoR分別為8.3個月和6.9個月,ORR分別為28.9%和28.5%。帕博利珠組和安慰劑組發生3、4級AE分別為79%和75%,總體上,帕博利珠單抗聯合化療治療BTC安全性良好。
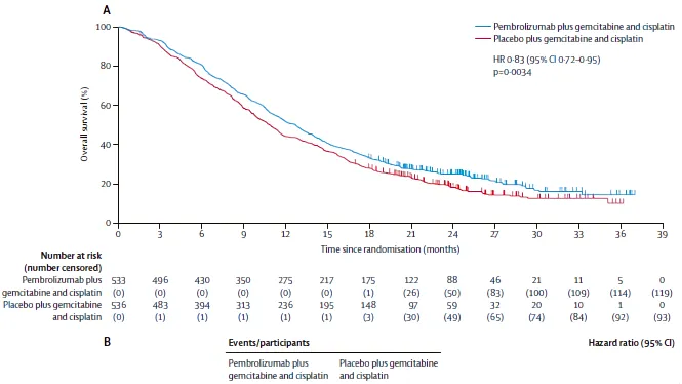
△ KEYNOTE-966研究OS數據。
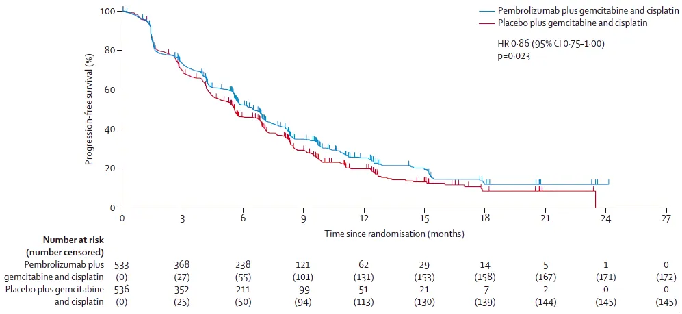
△ KEYNOTE-966研究PFS數據。
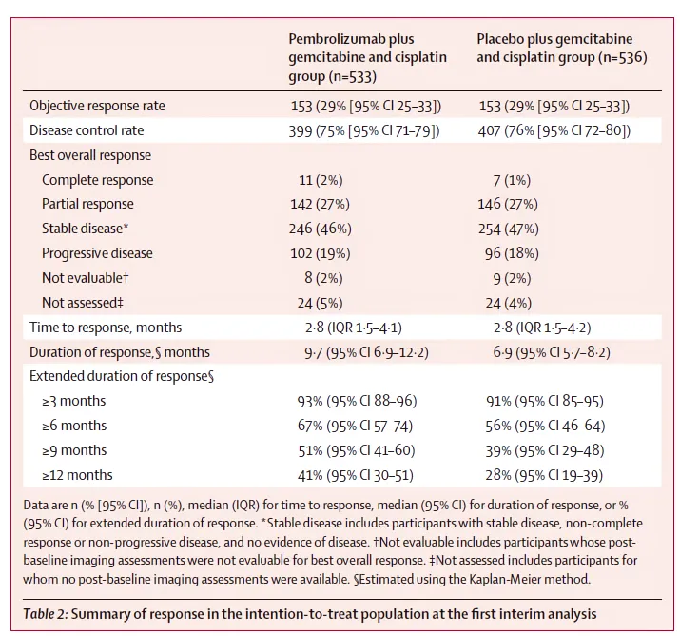
△ KEYNOTE-966研究臨床數據。
2024年1月至5月期間,消化系統腫瘤藥物的研究和開發取得了顯著進展,這些進展不僅包括了新藥的發現和臨床試驗結果,還涵蓋了治療方法的創新和藥物使用的優化。
這些進展的意義在于,它們不僅提高了消化系統腫瘤的治療效果,還促進了個性化和精準醫療的發展,同時也推動了全球腫瘤研究的合作與交流。
隨著新藥的不斷研發和治療方法的創新,患者的生存率和生活質量有望得到進一步提高。
大眾商報(大眾商業報告)所刊載信息,來源于網絡,并不代表本站觀點。本文所涉及的信息、數據和分析均來自公開渠道,如有任何不實之處、涉及版權問題,請聯系我們及時處理。大眾商報非新聞媒體,不提供任何互聯網新聞相關服務。本文僅供讀者參考,任何人不得將本文用于非法用途,由此產生的法律后果由使用者自負。
如因文章侵權、圖片版權和其它問題請郵件聯系,我們會及時處理:tousu_ts@sina.com。
舉報郵箱: Jubao@dzmg.cn 投稿郵箱:Tougao@dzmg.cn
未經授權禁止建立鏡像,違者將依去追究法律責任
大眾商報(大眾商業報告)并非新聞媒體,不提供任何新聞采編等相關服務
Copyright ©2012-2023 dzmg.cn.All Rights Reserved
湘ICP備2023001087號-2